SK케미칼이 자체 기술로 개발한 혈우병 치료제가 해외 선진 시장 공략을 앞두고 있다.
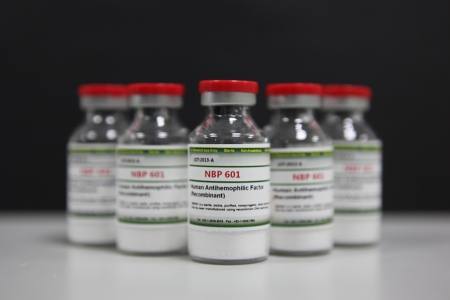
SK케미칼은 파트너사인 호주 바이오의약품 전문기업 ‘CSL’이 혈우병 치료제 바이오 신약 물질인 ‘NBP601(CSL627ㆍ사진)’에 대한 유럽의약품감독국(EMA) 시판 허가 신청을 완료했다고 23일 밝혔다.
SK케미칼에 따르면 국내에서 개발된 바이오 신약이 미국ㆍEU 등 해외 선진 시장에 허가를 신청한 것은 NBP601이 처음이다. 이는 SK케미칼이 자체 기술로 개발, 지난 2009년 호주 CSL에 기술 수출한 국내 최초 유전자재조합 바이오 신약 혈우병 치료제다. 2011년 IND 승인을 받은 이후 미국과 EU 등에서 글로벌 임상을 진행해 왔다.
NBP601은 A형 혈우병과 관련된 인자인 제8인자(factor VIII)의 안정성을 획기적으로 개선시킨 유전자재조합 바이오 신약이다. 특히 기존 제8인자에 비해 더욱 오랜 기간 동안 치료 효과를 보이는 것이 큰 장점으로, 글로벌 임상을 통해 EMA 승인에 필요한 모든 주요 평가 요건을 충족시켰다는 게 회사 측 설명이다.
A형 혈우병은 제8인자의 결함 혹은 결핍 등으로 발병되는 선천적 출혈성 장애 희귀질환으로, 유전적 결함 등으로 인체 내에서 혈액 응고인자가 만들어지지 않아 지혈이 잘 되지 않는 증상을 보인다. 현재 전 세계적으로 남성 약 5000~1만명당 1명이 앓고 있다.
혈액제, 바이오 시장 조사 전문 기업인 ‘MRB’ 조사 보고서에 따르면, 현재 A형 혈우병의 대표 치료제인 제8인자는 지난 2013년 기준 전 세계 64억 달러의 시장을 형성하고 있다. 이 중 재조합 제품의 매출은 2008년 39억 달러에서 2013년에는 51억 달러로 매년 5.9% 성장하고 있다.
특히 올해 초 토론토에서 열린 ISTH(혈액응고질환 관련 전문 국제학회)에서 공개된 임상 결과에 따르면 예방적 치료를 받은 환자들은 연간출혈빈도(ABR) 수치가 평균 1.14로, 기존 약물에 비해 40%가 개선된 것으로 나타났다. 또 연간자연출혈빈도(AsBR) 수치는 평균 0.0을 기록했다.
아울러 임상시험에서 전체 848건의 출혈 중 94%가 NBP601 2회 이하 투여, 그리고 81%는 NBP601 1회 투여로 출혈이 관리됐다. 이와 함께 출혈에 대한 지혈 관리도는 전체 835건 중 94%가 ‘매우 우수’ 또는 ‘우수’함을 보였다. 특히 A형 혈우병의 인자를 대체하는 치료법에서 가장 심각한 부작용인 중화항체반응은 단 한 건도 보고되지 않았다고 회사 측은 설명했다.
SK케미칼은 CSL와 유기적 협력을 통해 NBP601의 성공적인 글로벌 론칭을 위해 전사적으로 노력할 방침이다.
김훈택 혁신 R&D 센터장은 “지난 7월 미국 시장에 이어 이번 EU 시장 허가 신청이 완료됨으로써 회사의 R&D 기술력을 해외 시장에서 명실 공히 인정받은 것”이라며 “난치성 질환 정복을 위해 연구 중인 신약 후보물질의 임상시험을 성공적으로 마무리 해 R&D 혁신을 이어갈 것”이라고 밝혔다.













![밥상의 온기와 인간 중심 서사로 관객 사로잡은 ‘왕과 사는 남자’[리뷰]](https://img.etoday.co.kr/crop/85/60/2295902.jpg)







![2월 둘째 주 유튜브 영상 순위 [이투PICK 순삭랭킹]](https://img.etoday.co.kr/crop/300/170/2278370.jpg)
!['설 연휴 귀성차량으로 막히는 고속도로' [포토로그]](https://img.etoday.co.kr/crop/300/190/2296167.jpg)