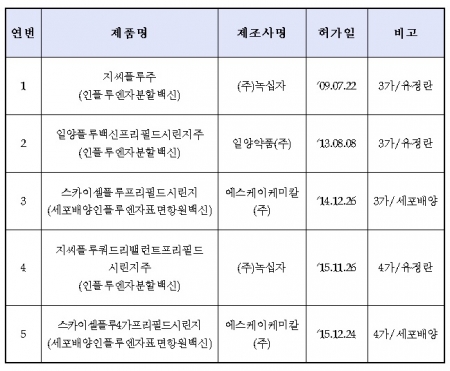
식품의약품안전처는 세포배양 방식으로 개발한 4가 인플루엔자 예방 백신인 ‘스카이셀플루4가프리필드시린지’를 세계 최초로 허가했다고 24일 밝혔다.
식약처에 따르면 이번 제품은 SK케미칼이 개발한 것으로, 1회 접종으로 A형 인플루엔자 바이러스 2종과 B형 인플루엔자 바이러스 2종 등 총 4종의 바이러스를 예방할 수 있는 4가 백신이다. 현재 우리나라·미국·유럽 등에서 허가된 세포배양 방식의 인플루엔자 예방 백신은 모두 3가 백신(A형 2종·B형 1종)이며, 4가 백신의 경우 모두 유정란(계란)을 사용한 제품들이다.
세포배양 방식의 제품은 계란을 사용하지 않아 생산량과 생산시기를 탄력적으로 조절할 수 있어 인플루엔자의 대유행 시 짧은 기간에 백신을 대량으로 신속하게 공급할 수 있는 장점이 있다. 특히 유정란 공급이 계란 백신의 생산량에 영향을 주는 것과 달리, 세포배양 백신은 원료 공급에 영향을 받지 않아 세포를 이용한 백신 개발이 가속화되는 추세다.
이번 제품은 만 19세 이상 성인 등을 대상으로 인플루엔자 예방 목적으로 허가됐으며, 세포배양 방식으로는 지난해 12월에 허가한 ‘스카이셀플루프리필드시린지(3가)’에 이어 2번째다. 또 국내에서 개발된 5번째 인플루엔자 예방 백신이기도 하다는 게 식약처 측 설명이다.
식약처 관계자는 “국내에서 최초로 4가 세포배양 백신을 개발·허가할 수 있었던 것은 정부가 운영하는 글로벌 백신 제품화 지원단을 통해 △허가·심사 △임상시험 △의약품 제조 및 품질관리기준(GMP) 등에 대해 맞춤형 컨설팅을 제공했기에 가능했다”고 밝혔다.
이 관계자는 이어 “백신 개발 및 제품화의 지원을 통해 백신 자급률을 높여 국내에서 인플루엔자 대유행과 같은 위기 상황에서 능동적으로 대응하는 동시에, 백신의 글로벌 시장 진출도 적극 지원할 예정”이라고 덧붙였다.



![올림픽이 너무 조용해요 [2026 동계올림픽]](https://img.etoday.co.kr/crop/140/88/2294154.jpg)
![직장인 설 상여금, 10명 중 4명은 받는다 [데이터클립]](https://img.etoday.co.kr/crop/140/88/2294169.jpg)







!["엔비디아가 골목길 입구까지 쫓아왔다?" 자율주행 사이다 팩트 체크 [찐코노미] #테슬라](https://i.ytimg.com/vi/tIWc3d9GgOE/mqdefault.jpg)








![직장인 설 상여금, 10명 중 4명은 받는다 [데이터클립]](https://img.etoday.co.kr/crop/300/170/2294169.jpg)
![김택우 의사협회장, 의대 정원 증원 관련 긴급 브리핑 [포토]](https://img.etoday.co.kr/crop/300/190/2294312.jpg)