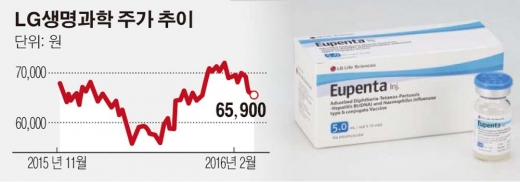
백신사업 경쟁력 강화에 나서는 LG생명과학의 행보에 힘이 실렸다. 5가 액상혼합백신 ‘유펜타(Eupenta)’가 세계보건기구(WHO)로부터 사전적격심사(PQ) 승인을 획득한 것. LG생명과학은 이를 통해 수출확대에 본격적으로 나설 계획이라고 밝혔다.
12일 금융감독원 공시시스템에 따르면 LG생명과학은 WHO로부터 5가 혼합백신 유펜타의 사전 적격성 심사를 승인받았다.
PQ 승인은 WHO가 의약품의 품질을 평가하는 심사로, 승인 획득 시 세계연합(UN) 산하 기관인 UNICEF 범미보건기구(PAHO) 등이 주관하는 국제 구호 입찰의 참여 및 공급 자격을 준다. 제조기술의 난이도와 검증된 원료 확보의 어려움 등으로 WHO PQ 승인을 보유한 업체는 세계적으로 6개사 정도에 불과하다.
LG생명과학은 이번 심사 승인을 계기로 4000억원 규모의 국제 입찰시장을 적극적으로 공략할 방침이다. 또한 남미, 아시아, 중동 지역으로 개별 수출에도 적극 나설 계획이다.
이를 위해 LG생명과학은 충북 오송에 860억원을 들여 백신 원제 생산시설도 설립할 예정이라고 밝혔다. 새로 설립되는 이 생산시설에서는 국내 기술로 개발한 5가 액상 혼합 백신 '유펜타'의 원료와 완제품을 생산하게 된다.
이에 금융투자업계에서도 긍정적인 평가를 하고 있다. 유펜타의 해외 수출이 매출성장으로 이어질 수 있을 것이란 분석에서다.
하태기 SK증권 연구원은 “올해 유펜타의 수출이 매출성장에 기여하며 전체 매출이 전년 대비 7.5% 증가한 4841억원을 기록할 것으로 추정한다”며 “영업이익도 9.6% 증가한 276억원을 기록할 것”이라고 예상했다.
김현태 KDB대우증권 연구원은 “자체 개발 제품인 유펜타가 수익성 개선을 견인할 것”이라며 “특히 올해 수출이 전년 대비 6.2% 늘은 2013억원을 기록할 것으로 추정한다”고 말했다.
한편, LG생명과학은 차세대 백신사업에도 역량을 집중하고 있다. 올해 6가 혼합백신과 폐렴백신 등 국제입찰시장용 백신의 임상시험에 진입할 계획인 것. 현재 개량형 혼합백신과 신규 폐렴백신 등 프리미엄 시장용 백신도 개발 중이다.

![[단독] '폴리우레탄' 원료값 60% 올랐다…가구·건자재·車 공급망 쇼크 [물류 대동맥 경화]](https://img.etoday.co.kr/crop/140/88/2313478.jpg)

![드디어 야구한다…2026 KBO 프로야구 개막 총정리 [해시태그]](https://img.etoday.co.kr/crop/140/88/2314015.jpg)
![한국인은 왜 하필 '쓰레기봉투'를 사재기할까 [이슈크래커]](https://img.etoday.co.kr/crop/140/88/2313851.jpg)


![전쟁·환율·유가 흔들려도… “주식은 결국 실적 따라간다”[복합위기 속 재테크 전략]](https://img.etoday.co.kr/crop/140/88/2313125.jpg)
!["리더십도 일관성도 부족"…국민의힘 선거 전략 어디로 [정치대학]](https://img.etoday.co.kr/crop/140/88/2313652.jpg)



![2차전지 판 제대로 열립니다! 4월 에코프로 놀라운 일 벌어질 수 있습니다 [찐코노미]](https://i.ytimg.com/vi/Xun283ivSCY/mqdefault.jpg)
![“코스피, 지수 높아도 가격 부담 낮아⋯거대 자금 쏠리는 조류에 올라타야”[와이즈포럼]](https://img.etoday.co.kr/crop/85/60/2314057.jpg)



![[오늘의 주요공시] 현대로템·한화시스템·효성ITX 등](https://img.etoday.co.kr/crop/85/60/2312693.jpg)
![[급등락주 짚어보기] 정부 양자암호통신망 구축 로드맵 발표에 우리로 '上'…6G·AI 관련주도 급등](https://img.etoday.co.kr/crop/85/60/2314030.jpg)

![[장외시황] 레몬헬스케어·폴레드, 코스닥 상장예비심사 승인](https://img.etoday.co.kr/crop/85/60/2314007.jpg)


![드디어 야구한다…2026 KBO 프로야구 개막 총정리 [해시태그]](https://img.etoday.co.kr/crop/300/170/2314015.jpg)
![‘와이즈포럼 - 시장 격변의 시대, 부동산·주식 투자전략은’ [포토]](https://img.etoday.co.kr/crop/300/190/2314064.jpg)