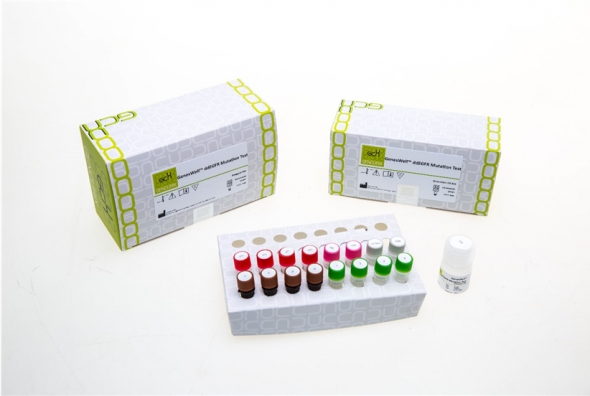
젠큐릭스는 21일 자사의 ‘GenesWell ddEGFR Mutation Test’가 티로신 키나아제(Tyrosine kinase) 저해제 투약이 가능한 비소세포성 폐암 환자 선별을 위한 동반진단검사로 식품의약품안전처로부터 3등급 의료기기 품목허가를 획득했다고 밝혔다.
이번에 허가를 받은 GenesWell ddEGFR Mutaion Test는 티로신 키나아제 활성을 억제하는 표적항암제의 약물반응성과 연관이 있는 EGFR 유전자 돌연변이를 46개까지 검출할 수 있으며, 이 중에는 3세대 약물 반응성을 예측할 수 있는 C797S 돌연변이가 포함된다. 또한 제품에 적용한 드롭렛 디지털 중합효소 연쇄반응(Droplet digital PCR; ddPCR) 기법으로 인해 극소량의 DNA만으로도 정확한 검사 결과를 도출할 수 있고 돌연변이에 대한 정략적 측정이 가능하다.
젠큐릭스는 비소세포성 폐암 환자군 검체를 대상으로 한 임상시험에서 해당 제품이 폐암 표적 항암제 ‘타세바(Tarceva, erlotinib) 처방에 필요한 상피세포수용인자 유전자 돌연변이 환자의 선별에 효과적임을 입증했고, 그 결과를 바탕으로 식약처로부터 동반진단검사 승인을 받았다.
조상래 젠큐릭스 대표는 “항암제동반진단사업단 성과물 중 하나인 GenesWell ddEGFR Mutation Test의 국내 허가를 통해 비소세포폐암 환자들에게 보다 정확한 치료 지표를 제공하게 되어 기쁘다. 앞으로도 다양한 암 종 및 암 유전자에 대한 동반진단 제품을 개발해 환자들에게 정확한 맞춤형 치료를 제공하기 위해 노력할 것”이라고 밝혔다. 그는 동반진단이 환자 삶의 질 향상 뿐 아니라 국가 보험재정 건전성에도 큰 기여를 할 수 있을 것이라고 덧붙였다.





![트럼프, ‘중국 원유망’ 정조준...미중 정상회담 ‘먹구름’ [호르무즈에 갇힌 경제 안보]](https://img.etoday.co.kr/crop/140/88/2301732.jpg)















![2월 넷째 주 유튜브 영상 순위 [이투PICK 순삭랭킹]](https://img.etoday.co.kr/crop/300/170/2278370.jpg)
!['중동 리스크' 흔들리는 환율…정부, 모니터링 강화 [포토]](https://img.etoday.co.kr/crop/300/190/2301765.jpg)