현재 세계에서 유일하게 위암 신약 임상 3상이 진행중인 아파티닙이 중국 내 간암, 폐암을 적응증으로 한 시판허가도 청신호가 켜졌다는 평가다.
11일 에이치엘비에 따르면 아파티닙은 올해 7월에 중국 내 보험급여의 적용이 결정되며 기존 시장 내 점유율이 10% 미만에서 30%까지 큰 폭으로 상승할 것으로 예상되고 있다.
현재 위암 3차 치료제로는 전세계에서 아파티닙이 유일하며, 대장암 3차 치료제, 간암 2차 치료제의 표준치료법으로 올해 승인받은 표적항암제 스티바가(Stivarga)는 임상결과 3급 이상의 부작용이 투약한 환자의 50.0%에서 나타나는 등 부작용이 적지 않다고 알려져 있다.
에이치엘비의 자회사 LSKB가 진행중인 글로벌 3상은 위암 3차 치료제를 적응증으로 시작한지 약 5개월만에 25%의 환자등록을 마쳐 내년 중에는 임상을 종료할 수 있다는 것이 회사의 예상이다.
특히 신라젠, 셀트리온, 삼성바이오로직스, 영진약품 등과 함께 바이오 관련주로 꼽히는 에이치엘비는 아파티닙에 대한 관련 논문 및 해외 저명한 투자자문회사의 전문 리포트들이 최근 쏟아지고 있다.
지난 8월 독일최대은행 도이치은행(Deutsche Bank)은 리포트를 통해 아파티닙과 비교되는 경쟁약물은 화이자의 수니티닙(Sunitinib, 오리지널약명 한국화이자의 ‘수텐’)이라고 분석했다.
뉴욕에 본사가 있으며 홍콩 런던 등 전세계에 영향을 미치는 투자자문회사 샌포드 앤 번스타인 (Sanford C. Bernstein & Co) 에서는 아파티닙의 간암, 폐암에 대한 2018년 예상 매출을 밝히며 두 적응증에 대한 시판허가 가능성을 전망했다.
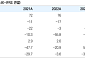
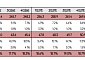
샌포드 앤 번스타인은 아파티닙의 간암 매출액은 2022년에는 11억1200만(1921억여 원) 위안까지 상승할 것이라고 예측했다. 또 폐암의 매출액은 2022년에는 5억5500억(1000억여 원) 위안으로 상승할 것으로 예측했다.
진양곤 에이치엘비 대표는 “최대한 빠른 시일 내 전세계 시장에서 시판허가를 받는 것을 목표로 하고 있다” 며 “일단 시장에 진입하면 병용요법을 필두로 다양한 적응증에 처방되기 시작될 것” 이라고 말했다.





![95% 치료제 없는 ‘이 분야’…K바이오에 기회될까 [800兆 희귀질환 시장]](https://img.etoday.co.kr/crop/140/88/2299281.jpg)
![출근길 짙은 안개·빙판길 주의…낮부터 포근 [날씨]](https://img.etoday.co.kr/crop/140/88/2242898.jpg)
![개미도 비상장 벤처 투자… 내달 'BDC' 첫선[개인 벤처투자路①]](https://img.etoday.co.kr/crop/140/88/2299217.jpg)
![“부산까지 2시간 30분"...인천발 KTX 직결 [집값은 철길을 타고④]](https://img.etoday.co.kr/crop/140/88/2299298.jpg)



![현대차 주가, 이제 '숫자'로 보지 마세요. 삼성전자보다 무서운 진짜 이유 [찐코노미]](https://i.ytimg.com/vi/TfLr6_Ne1wA/mqdefault.jpg)





![[오늘의 투자전략] 관세 흔들림에도 AI 불안 진정…코스피 6000선 재도전](https://img.etoday.co.kr/crop/85/60/2297483.jpg)

!["다같이 단종 안아"⋯'왕사남', 과몰입 비결 탈탈 털어보니 [엔터로그]](https://img.etoday.co.kr/crop/300/170/2299262.jpg)
![국민의힘, 상법 개정안 필리버스터 '돌입' [포토]](https://img.etoday.co.kr/crop/300/190/2299313.jpg)