증상은 10~21일 만에 정상으로 회복돼
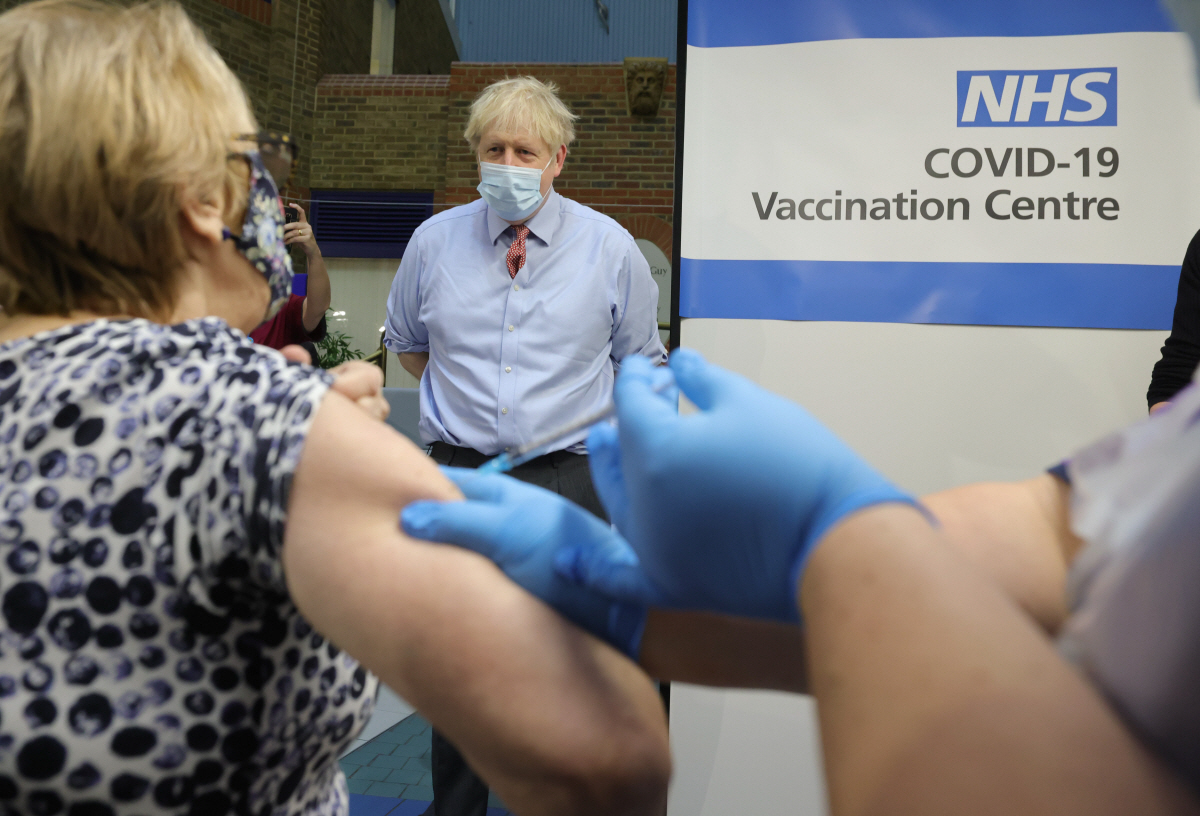
미국 식품의약국(FDA)은 10일 화이자 백신에 대한 긴급사용 승인 여부를 결정한다. FDA는 이에 앞서 전날 화이자가 미국과 독일, 터키, 남아프리카공화국과 브라질, 아르헨티나에서 약 4만4000명을 대상으로 한 마지막 임상시험 3상에서 나온 부작용과 효능 등을 평가한 53페이지의 보고서를 공개했다.
FDA에 따르면 임상시험 참가자 중 실제 백신을 투약한 2만1720명 중 4명이 안면마비 증세가 나타났다. 반면 위약 투약 그룹 2만1728명 중에는 이 증상이 전혀 나타나지 않았다. 보고서에 따르면 안면마비는 위약 그룹보다 백신 그룹에서 더 많이 발생한 유일한 부작용이었다.
그러나 FDA는 “백신 실험에서 발견된 안면마비 빈도는 일반 인구의 예상 유병률과 비슷하다”며 “백신과 연관이 있는 것으로 보이지는 않는다. 그러나 앞으로도 이를 면밀히 주시할 것”이라고 설명했다.
세계 최초로 화이자 백신을 접종하기 시작한 영국은 인구 10만 명당 안면마비 환자가 20~30명 정도로 임상시험에서 나타난 비율과 비슷하다. 영국 의약품건강관리제품규제청(MHRA)은 “화이자 백신은 다른 일반적인 백신과 비슷하다”며 “안전과 품질, 효능에서 우리 기준을 충족했다”고 강조했다.
부작용이 발생한 사람 중 1명은 접종한 지 3일 안에 안면마비 또는 얼굴 근육이 약해지는 증상을 보였다. 다른 한 명은 접종 후 9일 만에 안면마비가 일어났고 너머지는 각각 37일과 48일 만에 증상이 발생했다.
이들은 각각 10~21일 만에 안면마비에서 회복했다. 그러나 갑자기 증상이 나타나 뇌졸중이 나타난 것은 아닌지 우려됐다고 증언했다.





![‘탈미국’ 베팅 멈춤…해외 증시·채권 동반 급락 [전쟁이 바꾼 돈의 흐름 ①]](https://img.etoday.co.kr/crop/140/88/2311472.jpg)

!['국제 강아지의 날'…강아지에게 가장 묻고 싶은 말은 "지금 행복하니?" [데이터클립]](https://img.etoday.co.kr/crop/140/88/2311369.jpg)








![M7·S&P500 ‘디커플링’…빅테크 재부상 신호 [전쟁이 바꾼 돈의 흐름 ②]](https://img.etoday.co.kr/crop/85/60/2311476.jpg)
![‘탈미국’ 베팅 멈춤…해외 증시·채권 동반 급락 [전쟁이 바꾼 돈의 흐름 ①]](https://img.etoday.co.kr/crop/85/60/2311472.jpg)





!['검은 월요일' 코스피 6% 넘게 급락 [포토로그]](https://img.etoday.co.kr/crop/300/190/2311425.jpg)