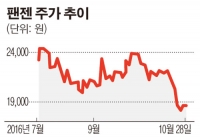
27일 팬젠에 따르면 연내 말레이시아에 EPO 제품허가등록신청서(NDA)를 제출하고, 내년 1분기에는 국내에 제출할 계획이다.
회사 관계자는 “말레이시아와 한국에 약 3개월 간격으로 NDA를 제출할 예정”이라며 “당초 사업을 계획했던 대로 순조롭게 진행되고 있다”고 말했다. 이어 “NDA를 제출하고, 최종승인이 되면 공시할 계획”이라고 덧붙였다.
구체적인 자료나 결과가 나오지 않으면 NDA를 제출하기 어렵다는 점을 고려했을 때, 팬젠의 NDA 제출 계획이 예정대로 진행되고 있다고 밝힌 것은 사업에 대한 자신감을 표현한 것으로 해석된다.
EPO는 신체의 산소 요구량에 따라 적혈구 생성을 조절하는 생체물질로 빈혈환자에게 사용하는 1세대 단백질의약품이다. 팬젠은 현재 말레이시아 국영 제약사인 CCM의 자회사 듀오파마(Duopharma)와 공동으로 다국적 임상 3상 시험을 진행하고 있다.
팬젠은 말레이시아, 브루나이, 싱가포르에 대한 EPO 판권계약을 체결했고, 터키와 태국에 대한 마케팅 계약도 맺은 상황이다. 이들 아세안국가의 2013년 EPO 시장규모는 약 2100억 원에 이르며, 2018년에는 2800억 원 규모에 이를 것으로 전망된다. 팬젠이 개발중인 바이오시밀러 EPO 제품의 국내 경쟁사는 CJ헬스케어, LG생명과학 등이 있으며, 해외에는 산도즈(Sandoz), 얀센(Janssen) 등이 있다.
김재윤 하나금융투자 연구원은 “팬젠의 EPO 치료제는 세계 두 번째 바이오시밀러 제품으로 내년 태국·터키, 2018년 베트남·필리핀·인도네시아 등 매년 진출시장을 확대해 나갈 것으로 기대된다”며 “올해 4분기부터 EPO의 판매가 시작돼 EPO 매출이 온기로 반영되는 2017년부터 팬젠의 영업이익은 약 100억 원을 달성할 것으로 기대된다”고 분석했다.
한편, 팬젠은 바이오시밀러의 개발·생산으로 하는 바이오기업이다. 팬젠이 보유하고 있는 바이오의약품 생산용 세포주 개발과 CHO세포에 특화된 단백질 발현기술을 기반인 ‘PanGen CHOTECH’를 기반으로 EPO(빈혈), FactorⅧ(혈우병), G-CSF(호중구감소증) 등의 바이오시밀러 제품을 개발하고 있다.
☞ 투자자 300명에게 공개하는 종목의 속살 이투데이 스탁프리미엄에서 확인하세요

![트럼프 ‘밀당’에 전 세계가 인질…‘전략적 혼란’의 정체 [이란 전쟁 한달]](https://img.etoday.co.kr/crop/140/88/2311613.jpg)

![2026 벚꽃 개화 시기·벚꽃 명소·벚꽃 축제 총정리 [그래픽 스토리]](https://img.etoday.co.kr/crop/140/88/2312008.jpg)
![“주택 업무 기피·시장 위축 우려” [공직 다주택자 딜레마 ②]](https://img.etoday.co.kr/crop/140/88/2310382.jpg)






![가격 폭등 호재 터졌다! 삼성전자 '이때까지' 걱정 없습니다[찐코노미]](https://i.ytimg.com/vi/dM_Z4acf1x8/mqdefault.jpg)



![[채권마감] 불스팁, 유가하락에 전날 패닉장 되돌림](https://img.etoday.co.kr/crop/85/60/2311991.jpg)



![[오늘의 주요공시] HD현대마린엔진·대신증권·SK이노베이션·셀트리온 등](https://img.etoday.co.kr/crop/85/60/2306877.jpg)


![2026 벚꽃 개화 시기·벚꽃 명소·벚꽃 축제 총정리 [그래픽 스토리]](https://img.etoday.co.kr/crop/300/170/2312008.jpg)
![외식물가 또 올랐다…자장면 0.5%, 칼국수·삼겹살 0.4%↑ [포토로그]](https://img.etoday.co.kr/crop/300/190/2311985.jpg)