지난 27일 식품의약품안전청은 대표적 비만치료제 성분인 오르리스타트에 대해 중증 간손상이 우려된다며 의약품 복용 후 간손상 징후가 나타나면 사용을 중지하는 내용을 담은 의약품 안전성 서한을 배포했다.
이는 최근 미FDA가 오르리스타트와 중증 간손상에 관한 모든 데이터를 검토해 최종적으로 중증 간손상 사례 13건이 확인됐다고 발표한데 따른 조치다. 그러나 아직 국내에서는 복통, 설사 등 25건의 경미한 사례만 보고됐을 뿐 심각한 간손상 사례는 없었다.
식약청은 오르리스타트를 복용하고 있는 환자에게 만약 '가려움, 피부 및 눈의 황달, 열, 무력감, 구토, 피로, 어두운 색 소변, 식욕 감퇴, 연한 색 대변' 등이 나타날 경우에는 간손상 징후 가능성이 있으므로 즉각 사용을 중단하라고 권고했다.
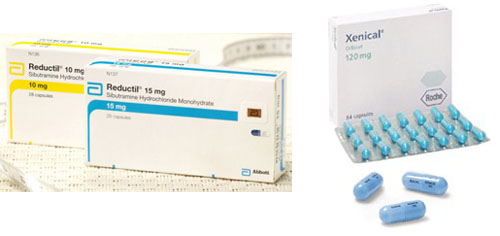
국내에서 오르리스타트 성분으로 만든 비만치료제는 로슈 '제니칼', 종근당 '락슈미캡슐', 한미약품 '리피다운캡슐', 드림파마 '올리엣캡슐', 비알엔사이언스(전 보람제약) '제로엑스캡슐' 등이 판매되고 있다. 한편 오르리스타트는 과거에도 경련 부작용이 보고돼 논란이 일기도 했다.
이에 앞서 식약청은 지난 1월에 시부트라민 성분의 비만약에 대해서 심혈관계 부작용 우려가 있다며 처방, 조제 자제를 당부하고 이어 2월1일에는 심장박동수가 지속적으로 증가하거나 치료 시작 후 3~6개월 내 체중이 줄어들지 않으면 투여를 중단할 것을 권고하는 안전성 서한을 배포했다.
이는 유럽의약품청(EMEA)이 대표적 시부트라민 성분약인 애보트 리덕틸에 대해 심장 관련 위험이 너무 크다며 판매중지를 요청한 것에 따른 것이다.
식약청은 이어 지난 3월 1년 이상 사용을 금하고 65세 이상 및 16세 미만에 대해서도 사용을 금지하는 내용을 중심으로 시부트라민 제제의 허가사항을 변경하고 안전성 서한을 배포했고 심혈관계 부작용에 대해서는 7월중에 최종결론이 나올 것으로 보인다.
현재 국내에서 시부트라민 성분이 든 비만약은 씨제이제일제당 '디아트라민', 유한양행 '리덕타민', 동아제약 '슈랑커', 한미약품 '슬리머' 종근당 '실크라민, 대웅제약 '엔비유' 등 상위사들이 대거 포함돼 있다.
시부트라민은 혈중 세로토닌 농도를 높여 식욕을 억제하고 오르리스타트는 지방분해효소인 리파아제가 지방과 결합하는 것을 차단해 지방을 변으로 배출시키는 약으로 항정신성 비만약을 제외하면 비만약 치료제 시장에서 양강체제를 구축하고 있다.
업계 관계자는 "비만치료제 부작용은 대부분 이미 허가사항에 기재돼 있고 인과관계가 확실하게 드러나지도 않은 상황"이라며 "약을 처방할 때도 의사들이 운동과 병행한 다이어트를 권고하고 있는 것처럼 비만약은 보조제로서 사용하는 것이 바람직하다"고 밝혔다.












![최태원, 李대통령 '가짜뉴스' 지적에 "재발 없도록 만전" 지시 [종합]](https://img.etoday.co.kr/crop/85/60/2292774.jpg)






![물가 안정세? 체감 어려운 이유⋯쌀ㆍ고기 비싼 탓 [물가 돋보기]](https://img.etoday.co.kr/crop/85/60/2290884.jpg)
![손발 차가워지고 색까지 변한다면⋯수족냉증’아닌 ‘이 질환’ [e건강~쏙]](https://img.etoday.co.kr/crop/85/60/2292506.jpg)
![키키도 소환한 그 감성⋯Y2K, 왜 아직도 먹히냐면요 [솔드아웃]](https://img.etoday.co.kr/crop/300/170/2292619.jpg)
!['노란 등불 밝힌 봄의 전령사' [한컷]](https://img.etoday.co.kr/crop/300/190/2292708.jpg)