오늘(24일)부터 바이오시밀러(바이오복제약)의 보험약가 산정 기준이 종전보다 14% 가량 인상된다. 셀트리온, 삼성바이오에피스 등이 현재 개발 중인 바이오시밀러 제품이 수혜를 입을 전망이다. 바이오시밀러 등재에 따른 오리지널 의약품의 인하 폭도 줄어들어 다국적제약사도 혜택을 기대할 수 있게 됐다. 국내에서 세계 최초로 허가받은 글로벌 혁신신약도 약가우대를 적용받는다.
24일 보건복지부에 따르면 지난 7월 발표한 ‘바이오의약품 및 글로벌 혁신신약 보험약가 개선안’과 ‘실거래가 약가인하제도 개선안’이 지난 6일 약제급여평가위원회에서 의결돼 24일부터 시행된다.
기존 약가제도와 가장 큰 변화를 살펴보면 바이오시밀러 제품의 약가 산정 기준이 다소 높아졌다. 국내 임상시험을 수행하고 혁신형제약기업이 개발하는 등의 요건을 충족한 바이오시밀러는 최대 오리지널 의약품 약가의 80%까지 받을 수 있게 된다. 기존 70%에서 10%포인트 높아졌다. 가격으로 보면 14% 인상되는 셈이다. 이때 오리지널 의약품의 보험약가도 기존 70%에서 80%로 상향 조정된다. 약가 우대 기간은 최대 3년이다.
보험상한가가 100원인 바이오의약품의 경우 바이오시밀러는 최대 70원까지 약가를 받을 수 있었는데 앞으로는 80원까지 산정 기준이 올라간다는 의미다. 오리지널 제품 역시 바이오시밀러 발매 이후 가격은 70원에서 80원으로 올라간다. 현재 바이오시밀러를 개발 중인 셀트리온, 삼성바이오에피스, LG생명과학 등이 모두 바이오시밀러 약가 우대를 적용받을 전망이다.
"한국 약가가 낮으면 해외에서 높은 가격을 받는데 걸림돌이 된다"는 바이오업체들의 약가 산정기준 상향 조정 요구를 수용해준 것인데, 국내업체보다는 다국적제약사들에 실익이 더 클 것이라는 분석이 나온다.
로슈의 유방암치료제 '허셉틴'이 대표적인 사례다. 허셉틴은 셀트리온의 바이오시밀러 '허쥬마'가 지난 2014년 1월 허가를 받으면서 약가인하가 예고된 상태다. 삼성바이오에피스도 허셉틴 바이오시밀러의 허가를 기다리는 중이다.
만약 약가제도 개편이 시행되는 24일 이전에 허쥬마의 약가가 등재됐다면 허셉틴의 약가는 30% 내려갈 예정이었다. 하지만 허쥬마의 약가 등재 이전에 개편안이 시행되면서 허쥬마 약가가 등재되더라도 허셉틴의 약가 인하율은 20%로 축소된다. 허셉틴의 지난해 처방실적은 830억원이다. 이번 약가 개편으로 최대 3년 동안 연간 83억원의 손실을 피할 수 있다는 계산이 나온다.
다만 바이오시밀러 제품이 최대로 받을 수 있는 오리지널 의약품의 80% 수준으로 약가를 등재할지는 미지수다.
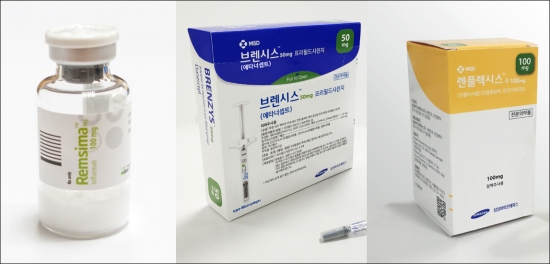
국내에 발매된 항체 바이오시밀러 ‘램시마’, ‘브렌시스’, ‘렌플렉시스’ 등 3종 모두 오리지널보다 5% 저렴한 약가로 등재됐다. 바이오시밀러를 오리지널과 같은 가격으로 시장에 발매하면 시장에서 경쟁력을 확보하기 어렵다는 이유에서다. 업계 한 관계자는 “바이오시밀러를 모두 80% 수준으로 올려도 오리지널 의약품만 80%로 상향될 뿐 바이오시밀러 업체는 큰 수혜는 크지 않을 수 있다”고 지적했다. 이러한 이유로 환자단체 등은 바이오시밀러의 약가산정 기준 인상을 반대했지만 복지부는 원안대로 의결했다.
이번 약가제도 개편을 통해 바이오베터의 약가 산정 기준도 신설됐다. 바이오베터는 이미 허가된 생물의약품에 비해 안전성ㆍ유효성 또는 유용성을 개선한 생물의약품을 말한다. 합성의약품에서 개량신약과 유사한 의미다. 한미약품의 약효 지속시간을 늘리는 '랩스커버리' 기술을 적용한 바이오의약품이 바이오베터로 분류될 수 있다.
기존에는 개량신약에 대한 약가 산정만 있었을 뿐 바이오베터에 대한 약가 산정 기준은 없었다. 복지부는 바이오베터의 약가를 개발목표제품 약가의 100~120%로 산정키로 했다. 합성의약품 개량신약의 약가 (개발목표제품 약가의 90~110%)보다 10%포인트 높은 기준이다.
바이오의약품의 함량을 늘린 제품에 대한 약가기준도 종전보다 높아진다. 예를 들어 주성분의 함량이 5%인 바이오의약품의 경우 주 성분 함량을 10%로 늘리면 보험약가는 5% 제품 대비 1.75배를 받을 수 있었다. 하지만 앞으로는 기존 제품 대비 1.9배의 가격을 받을 수 있다. 면역글로불린 등 바이오의약품을 많이 보유한 녹십자, LG생명과학, SK케미칼 등이 약가우대 수혜가 예상된다.
글로벌 혁신신약의 약가우대 조항도 새롭게 반영됐다. 복지부는 국내 보건의료 기여도가 높고 임상적 유용성을 개선한 신약에 대해 종전보다 약가를 높게 책정해주는 근거를 마련했다.
비용 대비 효과가 뛰어나다는 사실을 입증하는 경제성평가를 완료한 신약은 경제성평가 자료를 토대로 대체약제의 가격과 무관하게 보험약가를 설정한다. 경제성평가 자료를 내지 못하더라도 약가우대 혜택은 적용된다. 경제성평가를 진행하지 않거나 비용효과성을 입증 못한 신약은 대체약제 최고가보다 10%를 더 높게 책정해주기로 했다. 대체약제의 가격을 넘을 수 없다는 기존 상한선보다 가격을 높여준다는 의미다.
대체약제가 없다는 이유 등으로 경제성 평가 대상이 아닌 신약은 유사약제 A7(미국, 프랑스, 이탈리아, 독일, 일본, 영국, 스위스) 조정 최저가 수준으로 약값을 매긴다.
글로벌혁신신약은 건강보험심사평가원의 약제급여 평가기간이 120일에서 100일로 줄어들고 건보공단의 약가협상 기간도 현행의 절반인 30일로 단축된다.
글로벌혁신신약의 약가우대를 적용받으려면 국내에서 세계 최초로 허가, 국내에서 전 공정 생산, 환자치료지원 사업 등 사회적 기여도가 인정 등 세 가지 요건 중 하나를 충족한 신약에 한해 신약 허가를 위한 임상시험을 국내를 포함해서 실시하고, 혁신형제약기업ㆍ이에 준하는 기업ㆍ국내제약사-다국적제약사간 공동계약을 체결한 기업이 개발해야 한다는 요건을 충족해야 한다.
복지부 관계자는 “약가제도 개선으로 혁신신약 등 양질의 의약품을 개발하면 R&D 투자 확대 등 국내 보건의료에 대한 기여를 반영한 약가를 받을 수 있게 되고 보다 신속한 등재가 가능할 것으로 기대된다”고 말했다.




![전두환과 평행이론...윤석열 '내란죄 무기징역' 의미는? [인포그래픽]](https://img.etoday.co.kr/crop/140/88/2297723.jpg)









!["美 관세 판결 중기 영향 최소화"...중기부, 협·단체와 필요 조치 강구[美 상호관세 위법]](https://img.etoday.co.kr/crop/85/60/2297886.jpg)
![‘신격호 장녀’ 신영자 롯데재단 의장, 향년 85세 나이에 별세[종합]](https://img.etoday.co.kr/crop/85/60/2297979.jpg)

![[종합] 美 10% 대체 관세 신설…韓 전자·철강·車 ‘혼돈의 시간’ [美 상호관세 위법]](https://img.etoday.co.kr/crop/85/60/2155383.jpg)
![15% 무효, 10% 발효…전자·반도체 불확실성 고조 [美 상호관세 위법]](https://img.etoday.co.kr/crop/85/60/2297908.jpg)
![“당장 큰 영향은 없지만” K철강·배터리, 커진 불확실성에 고심 [美 상호관세 위법]](https://img.etoday.co.kr/crop/85/60/2290259.jpg)

![美 ‘상호관세’ 위법 판결에도…국내 車업계, ‘불확실성’ 오히려 커졌다 [美 상호관세 위법]](https://img.etoday.co.kr/crop/85/60/2295110.jpg)

![설 대목 지나도 농축산물 가격, 계속 오름세[물가 돋보기]](https://img.etoday.co.kr/crop/85/60/2297715.jpg)
![신혜선의 대형 사기극⋯부두아, 그래서 명품일까 아닐까 [솔드아웃]](https://img.etoday.co.kr/crop/300/170/2297799.jpg)
![매물 부족 심화…'전세 구합니다' [포토]](https://img.etoday.co.kr/crop/300/190/2297797.jpg)