외국계 제약사들이 신약을 들여와 국내 환자들을 상대로 한 임상시험에서 심각한 부작용이 발생한 것으로 드러났다.
특히 2006년 28건에 불과했던 약물 이상반응이 2010년 170건으로 6배 가량 늘어나 임상환자들의 각별한 주의가 요구된다.
25일 본지가 식품의약품안전청의‘2010년 임상시험 부작용사례’를 분석한 결과, 한국화이자, 한국얀센, 한국GSK, 한국MSD 등 국내 매출 10위권 안에 드는 제약사들이 다수 포함됐다.
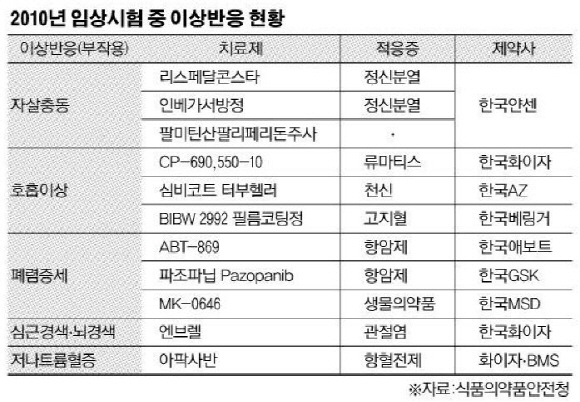
이들 제약사들은 자살시도, 호흡이상, 폐렴증세, 신근경색, 뇌경색 등의 중증 이상의 부작용을 보였다. 먼저 자살충동 부작용에서는 한국얀센 3건이 기록됐다. 정신분열증치료제 ‘리스페달콘스타’과 ‘인베가서방정’,‘팔미틴산팔리페리돈주사’가 각각 부작용을 보였다. 호흡이상 부작용 역시 3건이 기록됐다.
한국화이자 류마티스치료제 ‘CP-690,550-10’과 한국아스트라제나카(AZ) 천식치료제 심비코트 터부헬러, 그리고 한국베링거 고지혈증치료제 ‘BIBW 2992 필름코팅정’이 부작용을 보였다. 폐렴증세를 보인 치료제도 있었다.
한국애보트 항암제 ‘ABT-869'와 한국GSK '파조파닙’, 그리고 한국MSD 생물의약품 ‘MK-0646' 등이다.
이밖에 한국화이자 관절염치료제 ‘엔브렐’은 심근경색을, 한국BMS 항혈전제 ‘아팍사반’은 저나트륨혈증 부작용을 보였다. 이 같은 부작용 사례에 대해 외국계제약사들은 대수롭지 않다는 반응이다.
한 제약사 관계자는 “세상에 완벽한 치료제는 없다. 임상을 통해 보완해 나갈 뿐”이라며 “어떤 치료제든 조금씩의 부작용 사례들은 있을 수 있다”고 말했다.
임상시험 중 부작용 사례 건수는 매년 증가하고 있다. 2006년 28건에서 2007년 97건, 2008년 83건, 2009년 108건, 2010년 170건을 기록했다. 2010년 이상반응 사례(170건)를 2006년 28건과 비교해 보면 무려 6배가량 늘었다.
한편 국내에 들어와 공식적으로 한국다국적의약산업협회(외국제약사 모임) 회원사에 가입해 마케팅 활동을 펼치고 있는 외국계제약사는 총 30개사로, 가입하지 않고 활동하는 제약사를 포함하면 모두 40여 개사가 된다.



![직장인 설 상여금, 10명 중 4명은 받는다 [데이터클립]](https://img.etoday.co.kr/crop/140/88/2294169.jpg)








!["엔비디아가 골목길 입구까지 쫓아왔다?" 자율주행 사이다 팩트 체크 [찐코노미] #테슬라](https://i.ytimg.com/vi/tIWc3d9GgOE/mqdefault.jpg)










![직장인 설 상여금, 10명 중 4명은 받는다 [데이터클립]](https://img.etoday.co.kr/crop/300/170/2294169.jpg)
![국회 본회의 ,경제분야 대정부 질문 [포토]](https://img.etoday.co.kr/crop/300/190/2294216.jpg)